
中国生物医药不仅在仿制药市场占有一席之地,也成为全球第二大新药开发国,仅次于美国。其在政府支持下,所采取在现有药物基础上改进的「快速跟进」以及通过授权交易稳定资金来源的策略,在创新药物研发上展现强大的竞争力,让全球惊艳。
中国生物医药产业迅速崛起,凭借低成本、高效率的研发优势,一批生物医药民企在国际舞台上崭露头角,吸引海外公司频繁交易。据投行Stifel数据,2024年大型制药公司授权交易中,有三成来自中国,两年前这个数字为12%。美国媒体直言「中国创新药迎来DeepSeek时刻」,意思是除了AI(人工智能)领域,中国在生物医药领域同样有了世界级突破性进展。
据大公报报导,近年来,中国通过一系列政策全面支持生物医药企业以及产业全链条创新发展。今年1月,国务院办公厅印发「关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见」,为健全支持创新药和医疗器械发展的监管体系、机制提出具体指引。
2024年7月,国务院发布「全链条支持创新药发展实施方案」,提出要全链条强化政策保障,统筹用好价格管理、医保支付、商业保险、药品配备使用、投融资等政策,优化审评审批和医疗机构考核机制,合力助推创新药突破发展。
药物授权国际药厂
在一系列政策支持下,愈来愈多的中国生物科技企业开始向全球制药巨头授权自主研发的药物,标志着中国在全球医药产业中的影响力不断增强。
今年2月6日,上海生物医药企业复宏汉霖发布公告,该公司与世界上最大的仿制药制造商之一、印度制药企业瑞迪制药(Dr. Reddy’S Laboratories S.A.),就自主开发用于治疗多发性骨髓瘤的在研达雷妥尤单抗生物类似药HLX15(重组抗CD38全人单克隆抗体注射液)签署授权许可协议,达成在研生物类似药HLX15欧美市场授权,这项授权交易总金额超过1亿美元。
复宏汉霖首席商务发展官兼高级副总裁曹平表示,HLX15是强生达雷妥尤单抗生物类似药候选药物。根据IQVIA(全球最大制药咨询服务公司之一)最新数据,2023年,达雷妥尤单抗于全球范围内的销售额约为106亿美元。

目前全球尚未有达雷妥尤单抗生物类似药获批上市,HLX15有望成为全球首个达雷妥尤单抗生物类似药,「HLX15的差异化布局,叠加合作伙伴的本地化经验,将为中国生物药的全球竞争力提供新范式」。
除了复宏汉霖,过去两年,包括阿斯特捷利康、GSK和默沙东在内的大型制药集团都与中国生物技术公司签署了价值10亿美元以上的授权协议,中国生物药企业的竞争力愈来愈强。
美国「华尔街日报」早前的一篇报导透露,美国生物制药公司Summit Therapeutics去年宣布,其一款新药在肺癌治疗试验中打败了美国默克公司的一款最畅销的抗癌药物。
其中值得注意的是,该新药是由一家中国生物科技公司研发并授权。「华尔街日报」报导对此描述:「这一结果是生物科技行业的分水岭,来自中国的竞争力凸显」。
从一系列数据不难发现,来自中国的竞争直追美国。据投行Stifel的数据,2024年大型制药公司的授权交易中,有三成来自中国,两年前这个数字为12%,而这一势头有望在今年持续。

生物医药行业研究机构DealForma数据显示,2020年,在价值5000万美元或以上的医药行业交易中,涉及中国的比率还不到5%;而这个比率在2024年已经上升到近30%。Stifel预计十年后,许多进入美国市场的药物将源自中国实验室。
高盛发布了一篇关于中国生物科技的深度投资价值分析报告,表示持续看好中国医疗健康板块中的生物科技领域,中国创新力量正在并将持续获全球认可。该报告中还提及了再鼎医药、传奇生物、诺诚健华、百济神州和信达生物这些头部公司成为优选标的。展望2025年,中国企业有望在更广泛治疗领域的创新能力持续获得国际认可。
在中国生物医药行业赶超全球技术的过程中,企业自身的奋发图强发挥了至关重要的作用。报导指出,从其采访的生物制药、医疗器械等医药产业公司得知,研发过程往往艰苦而漫长,但在长期的积累与实践中,才能够不断完善技术和积累经验。
「生物类似药的开发过程昂贵且耗时,通常需要五至六年,根据对照组原研药的售价,开发费用可能高达2亿美元。」曹平表示,复星医药2月6日公告,截至2024年11月,集团现阶段针对HLX15累计研发投入约为人民币1.2亿元(未经审计)。根据本次合作约定,复宏汉霖将继续负责HLX15的研发并承担相应费用。
克服人才、经费难关
曹平指出,新药研发在技术和工艺的复杂性、全球注册申报、大规模国际多中心临床试验开展、国际化规模生产和质量控制等方面均面临着重重挑战。
她还举例道:「以生物类似药药学研究(CMC)阶段的挑战为例,生物类似药的工艺开发需与原研药高度一致,由于生物类似药是由活细胞或生物体制备的,其生产过程非常复杂,对工艺变化非常敏感,分子结构可能会随着生产过程的变化而变化,对最终的产品质量、纯度、生物特性以及临床效果产生较大的影响」。
除了制药公司,生物医药产业中的医疗器械领域企业也表达了自主研发新产品的难度和风险。
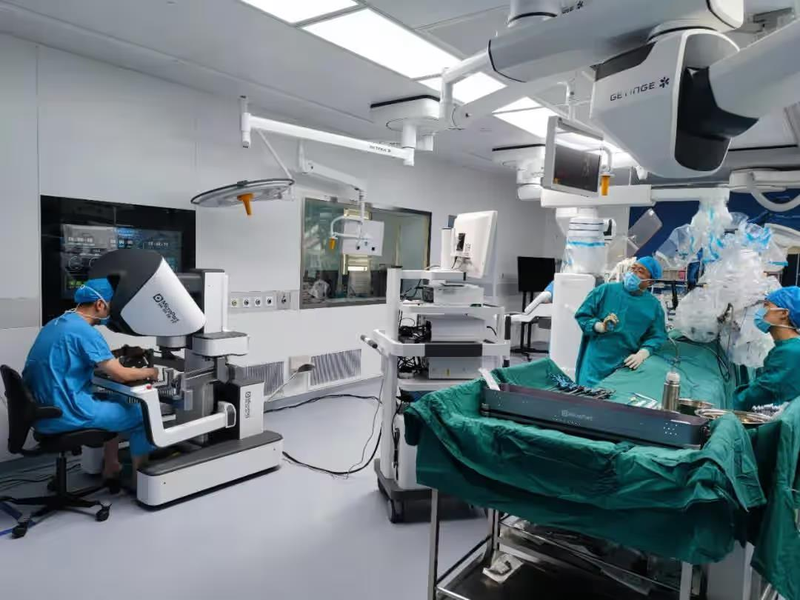
上海微创医疗机器人(集团)股份有限公司自主研发的图迈单孔腔镜手术机器人,早前正式获得国家药品监督管理局批准上市。公司相关负责人表示,他们一切都是从零开始,所以在前面的5年时间里,一直是集中力量攻克最艰难的技术。
「其间,包括控制器、内窥镜、软件算法等在内。没有人才,就自己培养;缺少产业配套,就自己摸索;需要技术方向,就去医院反复和临床医生商讨。经过多年研发创新与产业积累才有今天的成果」,这位负责人表示。
AI重塑产业生态 从「跟跑」转向「并跑」
对于中国医药行业进入自主研发高光期,曹平表示:「我们看到中国医药创新已逐渐从『跟跑』转向『并跑』。政策与资本是引擎,技术是燃料,三者合力促使实现从『中国新』到『全球新』的跨越」。
当然,企业的努力也不可忽视,就复宏汉霖而言,公司以抗体技术为内核,在生物大分子药物发现及优化、临床前研究、生产细胞株构建、上下游工艺开发、制剂开发、临床开发等方面经过长期积累,形成了完善且规范的全产业链技术平台。
同时,复宏汉霖成功构建了高效的一体化全球研发、药政注册及临床开发营运平台。截至目前,复宏汉霖已在全球范围内完成700余项药政注册申请,并获得500余项批准,覆盖中国、美国、欧盟、加拿大、印尼和日本等多个国家和地区,并在美国、欧盟、东南亚、日本等国家和地区开展国际多中心临床试验,加速产品全球化进程。
出海成为必经之路
上海微创医疗机器人相关负责人表示,出海已成为中国医疗器械企业必经之路,公司第一款出海内核产品是鸿鹄骨科手术机器人、图迈手术机器人,目前已经在全球多个国家完成商业化装机并进入临床应用。
「我们产品出海依靠的不是低价竞争,而是以创新技术、产品质量、客户服务以及临床价值极高的解决方案赢得客户信赖」,他表示。
复宏汉霖的出海战略则是通过「授权合作广度」与「自主创新深度」双轨并行,既输出创新能力和可负担高质量的研发范式,也在实现商业价值的同时,践行患者可及性使命。
曹平表示,真正的全球化创新必须根植于真实世界需求。当中国药企能用高质量数据提升患者生存时,这就是对「创新话语权」的最佳诠释。
报导指出,近年来,AI正在以惊人的速度重塑生物医药行业。通过大数据分析、机器学习和深度学习的深度融合,AI可以加速药物研发进程、减少投入成本等传统难题。尤其在中国,AI与生物医药的结合正成为推动产业升级的重要引擎,多家药企和科技公司相继有技术突破。
打破研发双十定律
实际上AI制药在国内并不罕见,甫康药业是一家将AI深度融入药物研发的中国企业,专注于抗肿瘤和抗衰老领域的药物研发和生产,该公司利用自主研发的Right 6D联合AI技术平台,在抗肿瘤领域取得进展,为广大肿瘤患者提供创新治疗方案。公司产品管线强劲,覆盖了乳腺癌、前列腺癌、胰腺癌、肝癌、胃癌、肺癌等国内外急需创新治疗方案的实体肿瘤。
在医药界有一个「双十定律」:一款创新药从启动研发到上市,平均成本超过10亿美元,研发时间超过10年,且约90%的药物会在临床试验阶段失败。晶泰科技作为国内AI制药的领军企业,技术突破了AI+量子计算重构药物研发逻辑,在药物发现阶段,其算法能够快速筛选潜在化合物并预测晶型稳定性,将早期研发周期缩短40%至60%。
中国AI制药的快速发展得益于多重因素。国家政策支持为行业提供了沃土。「『十四五』生物经济发展规画」明确提出,面向一系列重大疾病,依托人工智能技术、生物医学和健康大数据资源,发展智能辅助决策知识模型和算法,辅助个性化新药研发,为疾病诊断治疗提供决策支持。此外,华为、百度、腾讯、京东等科技巨头也纷纷布局AI,进一步丰富了行业生态。

英硅智能联合首席运行官任峰表示,2025年,AI制药领域有两大看点:一是临床里程碑将增多;二是围绕平台授权、CRO业务、管线交易等达成的大额交易将增加。
晶泰控股联合创始人赖力鹏认为,AI的内核价值在于帮助弥补「未知的未知」,通过强大的记忆和分析能力,为决策提供支持。以生物医药行业为例,AI技术展示了巨大潜力。传统药物研发面临「反摩尔定律」困境,如研发周期长、成功率低、成本高。AI技术通过全流程优化和多因素集成,显著提升研发效率。




